電気陰性度、聞いたことがあるなと思ったら、アルコールの水素結合のところで勉強していました。
電気陰性度(electronegativity)とは、原子が他の原子と結合するときにどれだけ自分のほうに電子を引き寄せるかを表す指標です。
イオン化エネルギーと電子親和力は原子単体に生じるエネルギーであるのに対し、電気陰性度は原子と原子が結合して分子となるときに電子を引っ張る力の大きさということになります。
周期表と電気陰性度
共有結合をしない18族の希ガスを除いて、周期表の右上に行くほど電気陰性度は強くなる傾向があります。
その理由として、以下の2点が考えられるようです。
- 原子が自分のほうに電子を引き寄せる力とは、原子の中の原子核、つまり陽子が電子を引っ張る力といえる。原子核からの距離が近いほど共有電子対をより強く引き寄せるため、周期表の上に行くほど電気陰性度は強くなる。
- 原子核の正電荷が強いほど共有電子対をより強く引き寄せるため、周期表の右側に行くほど陽子の数が増えて電気陰性度は強くなる。
分子の極性とは
例えば塩酸(HCl)では、水素(H)と塩素(Cl)が結合するときに電子を共有して共有電子対を作ります。 このとき、Hより電気陰性度の強いClのほうが強く電子を引き寄せます。
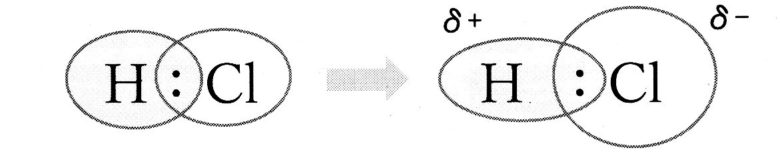
Hの電子雲がClの電子雲のほうにぐいっと引っ張られています。
HからClに電荷が偏っているため、Clはわずかにマイナス(δ-)の電荷を帯び、Hはその分だけマイナスの電荷が減ってわずかにプラス(δ+)の電荷を帯びています。
このように、共有結合している原子間に電荷の偏りがあることを極性といい、極性がある分子を極性分子といいます。
電気陰性度による水素結合
原子と原子が結合して分子を作るとき、電気陰性度の差が大きい場合、より強い極性を生じます。
特に強い極性を生じた結果、水素結合が作られます。
プラスとマイナスの電荷によって結合を作りますが、イオン結合とは異なり、電気陰性度の差によって作られる結合が水素結合です。
水素結合を作るのは以下の3つのケース:
フッ素(F)とH → HF

酸素(O)とH → H2O
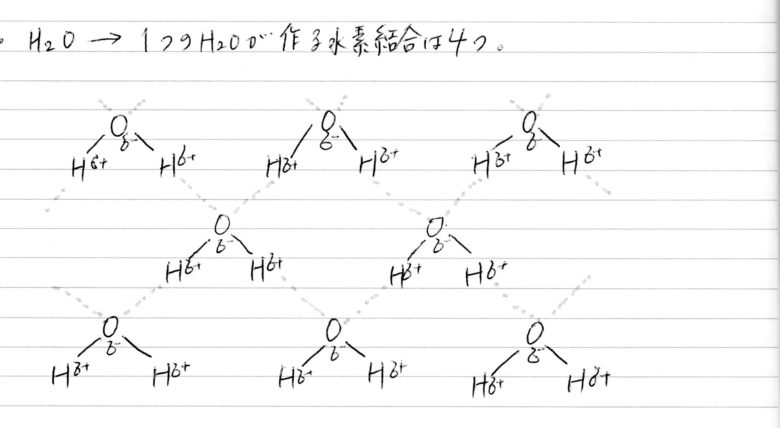
窒素(N)とH → NH3

水素結合は結合力が強いため分子がバラバラになりにくく沸点が高いということも有機化学編のアルコールの単元で学びましたね。
理論と有機がつながってきました!



コメント